به نظر میرسد عمدهی افراد کادر درمان در بیمارستانها، به علائم هایپرکالمی و تغییرات نوار قلب پتاسیم بالا مثل موج تی نوکتیز و بلند حساس هستند و به دنبال آنها میگردند. این موضوع عالی است؛ اما فراموش نکنیم که خطر هایپوکالمی اگر بیشتر از هایپرکالمی نباشد، کمتر نیست. باید حواسمان به علامتهای این اختلال الکترولیتی باشد و آنها را خوب بشناسیم. این نوشته، در مورد علائم بالینی هایپوکالمی و تغییرات نوار قلب مرتبط با پتاسیم پایین است.
توضیح: در عمده کتب رسمی، دو پیشوند Hypo و Hyper به شکل هیپو و هیپر نوشته میشود. در نتیجه دو عبارت هیپوکالمی و هیپرکالمی را زیاد میبینیم. ترجیح مدرسه پزشکی این است که این دو پسوند را به شکل هایپو و هایپر بنویسیم. معتقد هستیم اکنون در زبان روزمره کادر درمان اینقدر این دو تلفظ رایج شده که شکل نوشتاری را هم بخواهیم به این سمت ببریم و به تلفظ انگلیسی نزدیکتر شویم.
به طور کلی دو عامل بر بروز علائم در کمبود پتاسیم تأثیر میگذارد:
۱. شدت هایپوکالمی
قاعدتاً هرچه پتاسیم پایینتر باشد، احتمال علامتدار شدن بیمار بیشتر خواهد بود. معمولاً زمانی که پتاسیم به زیر ۳ میلیمول در لیتر میرسد فرد علامتدار میشود.
۲. زمانی که طول کشیده تا هایپوکالمی ایجاد شود
ممکن است پتاسیم بیماری بالای ۳ میلیمول در لیتر (برای مثال ۳/۲) باشد؛ اما فرد به دلیل کاهش سریع سطح پتاسیم علائم هایپوکالمی را از خود نشان دهد.
یا این که یک عامل مستعدکننده مثل مصرف دیگوکسین باعث بروز علائم شده باشد.
علائم کمبود پتاسیم (هایپوکالمی)
علائم بالینی هایپوکالمی را با توجه به اثرات آن در اعضای مختلف، میتوان در سه سطح بررسی کرد:
۱. پانکراس
در حالت عادی گلوکز وارد سلول شده و سپس تبدیل به گلوکز ۶ فسفات (Glucose-6-Phosphate) میشود. در مراحل بعدی، از این گلوکز، Adenosine Triphosphate یا ATP ساخته خواهد شد.
یک سری کانالهای پتاسیمی روی سلولهای بتا پانکراس وجود دارد. این کانالها به ATP حساس هستند. زمانی که سطح ATP در سلول افزایش مییابد، این کانالهای پتاسیمی بسته میشوند و در نتیجه خروج پتاسیم از سلول متوقف میشود.
به دنبال توقف خروج پتاسیم، بار مثبت در سلول تجمع یافته و درون سلول مثبت میشود و غشای سلول به پتانسیل آستانه (Threshold Potential) میرسد و پتانسیل عمل اتفاق میافتد. میدانیم که در عمدهی سلولها، رسیدن به پتانسیل آستانه، با ورود یک یون مثبت مثل سدیم یا کلسیم انجام میشود؛ اما در اینجا با عدم خروج پتاسیم است که سلول به پتانسیل آستانه میرسد و پتانسیل عمل آغاز میشود.
نتیجهی نهایی رسیدن به پتانسیل عمل و در نتیجه تغییر ولتاژ، باز شدن کانالهای کلسیمی حساس به ولتاژ است. پس، کلسیم وارد سلول میشود که منجر به ادغام وزیکول حاوی انسولین با غشا شده و انسولین ترشح میشود.
حالا اگر فرد دچار هایپوکالمی شده باشد و پتاسیم خارج سلولی کم باشد، تمایل پتاسیم برای خروج از سلول افزایش مییابد، یونهای پتاسیم درون سلول باقی نمیمانند و سلول حالت هایپرپلاریزهی به خود میگیرد. در نتیجه رسیدن به پتانسیل آستانه سخت میگردد و ترشح انسولین کم میشود. پس فردی که کمبود پتاسیم دارد، به علت کاهش ترشح انسولین ممکن است عدم تحمل گلوکز هم داشته باشد و قند خونش بالا برود.
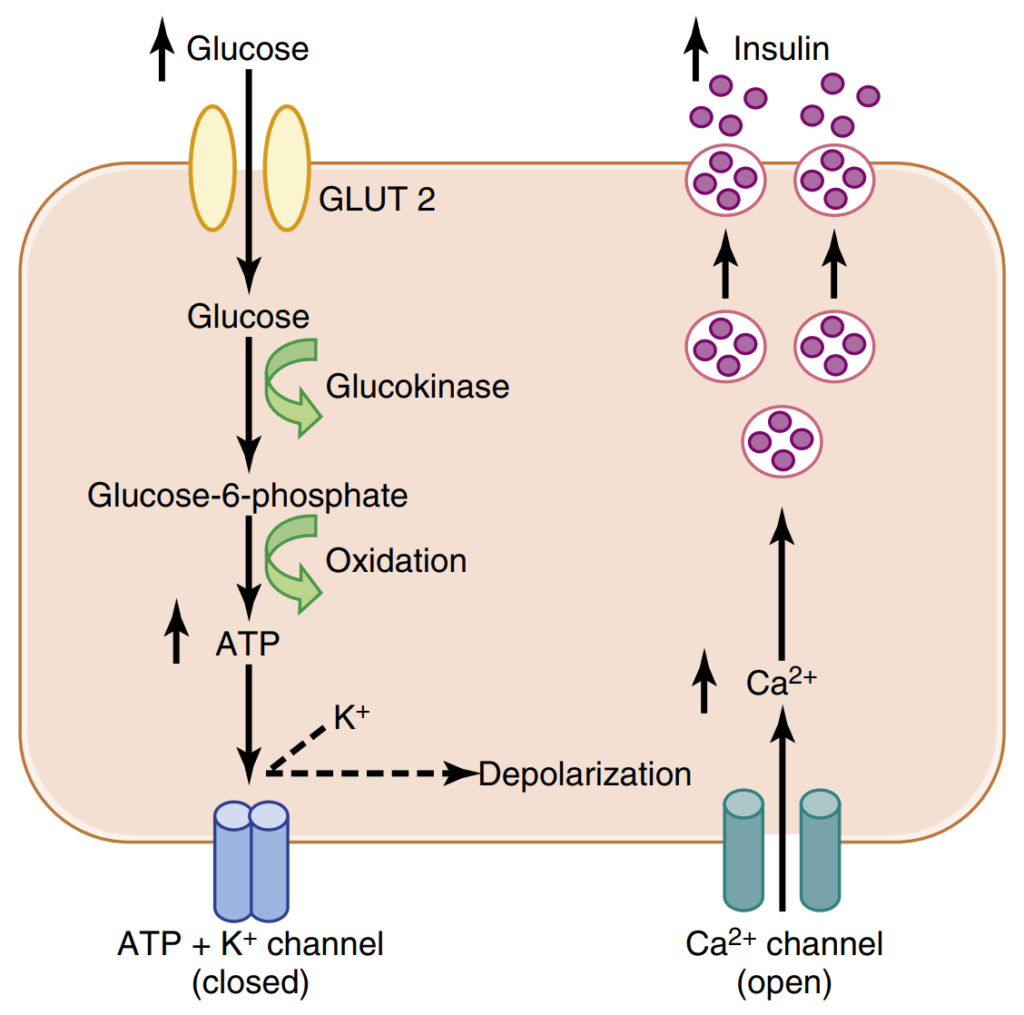
Guyton and Hall Textbook of Medical Physiology 14th edition; Chapter 79, Page 979
۲. کلیه
نفروپاتی هایپوکالمیک (Hypokalemic Nephropathy) از اثرات هایپوکالمی بر کلیه است. علت این نفروپاتی، آمونیاک بیش از حد است. پتاسیم پایین – اگر به خاطر شیفت به داخل سلول نباشد – منجر به افزایش آمونیاک خواهد شد.
مسیر ساخت آمونیاک در کلیه
مسیر شروع تولید آمونیاک در توبول پروگزیمال نفرون است. در این سلولها از گلوتامین، آمونیوم (+NH4) ساخته خواهد شد. آمونیوم به داخل توبول آمده و بعد دوباره در قسمت ضخیم بالاروندهی هنله بازجذب شده و تبدیل به آمونیاک میشود.
آنزیمهای ساخت آمونیوم از گلوتامین (مسیر Ammoniagenesis) به pH درون سلول حساساند و در صورت اسیدوز داخل سلولی (Intracellular Acidosis) بیشتر خواهند شد. پتاسیم پایین، منجر به اسیدوز داخل سلولی میشود. زمانی که سطح پتاسیم در خون کاهش مییابد، یون هیدروژن با یون پتاسیم مبادله میشود.
در نتیجه میزان یون هیدروژن داخل سلول افزایش مییابد و اسیدوز داخل سلولی خواهیم داشت. یادمان باشد که آمونیاک مهمترین بافر ادراری است و با اتصال به +H و تولید +NH4 منجر به دفع اسید از طریق ادرار میشود؛ اما همین آمونیاک برای کلیه آسیبزا نیز میتواند باشد.
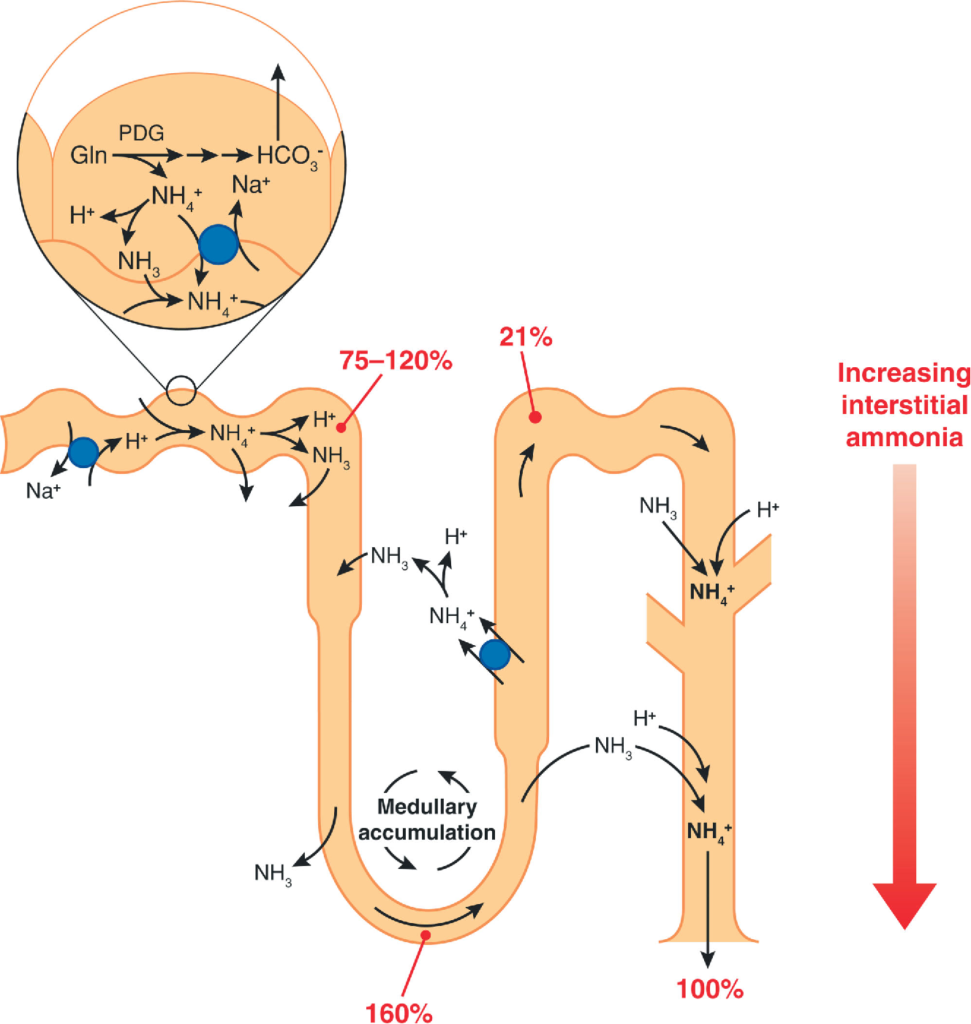
(منبع)
همچنین هایپوکالمی باعث دیابت بیمزهی نفروژنیک (یا همان مقاومت به ADH) میشود. این عارضه از طریق کاهش توانایی غلیظ کردن ادرار ایجاد میشود. در توبول هنله پروتئین معروف NKCC2 قرار دارد که یک یون سدیم، یک یون پتاسیم و دو یون کلراید را وارد سلول میکند.
این یونها بعد از ورود به سلول، وارد مدولا شده و آن جا را هایپراسمولار میکنند. ADH تنها یک کانال آب را روی غشا میگذارد. باید مدولای هایپراسمولاری وجود داشته باشد که هنگام وجود این کانال، آب را به داخل مدولا بکشد.
زمانی که پتاسیم کم باشد، این پروتئین نمیتواند تنها سدیم و کلر را وارد سلول کند. در نتیجه حتی اگر ADH اثر بگذارد و آکواپورین۲ (Aquaporin) روی غشا قرار بگیرد، آب زیادی بازجذب نمیشود و پرادراری (پلی اوری یا Polyuria) خواهد داشت.
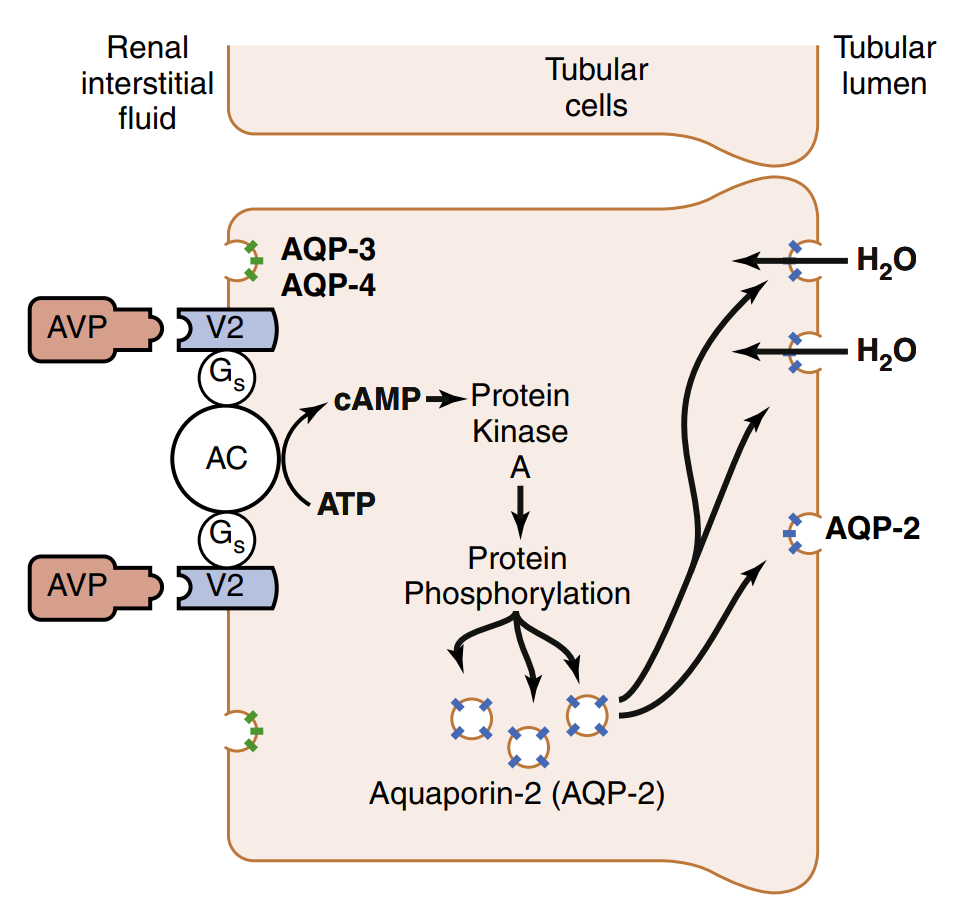
Guyton and Hall Textbook of Medical Physiology 14th edition; Chapter 28, Page 360
۳. ماهیچهها
هایپوکالمی بر روی هر سه نوع ماهیچهی قلبی، صاف و اسکلتی تأثیر میگذارد.
۳.۱. ماهیچه اسکلتی
هایپوکالمی باعث ضعف یا حتی فلج عضلانی میشود. الگوی آن مشابه ضعف عضلانیای است که در هایپرکالمی بروز مییابد. حالت صعودی (Ascending Paralysis) دارد؛ به این شکل که معمولاً از اندام تحتانی آغاز شده و پیشروی میکند و به تنه و در نهایت اندام فوقانی میرسد. در کنار این علائم، کرامپ عضلانی، میوگلوبینمیا و رابدومیولیز هم دیده میشود. علت ایجاد این ضعف عضلانی در قسمت ماهیچهی قلبی توضیح داده خواهد شد.
علت ایجاد رابدومیولیز در هایپوکالمی
در زمان فعالیت نیاز ماهیچه به خون افزایش مییابد. برای افزایش جریان خون عروق متسع میشوند. یکی از عوامل وازودیلاتور، پتاسیم است. پتاسیم با خروج خود از سلولهای ماهیچهای، باعث اتساع عروق و افزایش جریان خون میشود. زمانی که فرد هایپوکالمی شدید دارد، سلولها نیز دچار کمبود پتاسیم میشوند.
یادمان باشد که اگر علت هایپوکالمی شیفت به سلول نباشد، به ازای یک میلیمول کاهش پتاسیم خون، ۳۰۰ تا ۴۰۰ میلیمول از پتاسیم درون سلولی کم میشود.
به دنبال کمبود پتاسیم، آزادسازی آن از سلولهای ماهیچهای نیز کاهش مییابد و در نتیجه اتساع عروق رخ نمیدهد. در نهایت به علت نرسیدن خون کافی به عضلهی درحال فعالیت، رابدومیولیز ایسکمیک اتفاق میافتد.
نکتهی قابل توجه این است که یکی از علائم رابدومیولیز، هایپرکالمی است که در این موارد میتواند هایپوکالمی فرد را مخفی و تشخیص را برای پزشک سخت کند.
بررسی یک کیس رابدومیولیز ناشی از هایپوکالمی
خانمی ۶۲ ساله با اسهال شدید به بیمارستان مراجعه کرد و بستری شد. در بدو ورود پتاسیمهای پایین داشت. روز دوم بستری با آنکه هنوز آنقدر پتاسیم نگرفته بود که پتاسیم نرمال شود؛ اما در آزمایشها، پتاسیم نرمال، LDH و AST افزایش یافته داشت. به دنبال منشأ این LDH و AST گشتیم. دو منشأ محتمل، تخریب گلبول قرمز و تخریب عضله است. هموگلوبین بیمار افتی نداشت و در آزمایش روز اول CPK نرمال بود. CPK تکرار شد. در آزمایش روز دوم، افزایش شدید CPK به بالای ۵۰۰۰ واحد در لیتر داشت. با توجه به CPK بالا، منشأ LDH و AST نیز از عضله بود. به خاطر پتاسیم پایین مبتلا به رابدومیولیز شد و آزاد شدن پتاسیم به دنبال رابدومیولیز، پتاسیم پایین را مخفی کرد.
۳.۲. ماهیچه صاف
هایپوکالمی با اثر بر ماهیچههای گوارشی، علائمی را در این سیستم ایجاد میکند و میتوانیم به خاطر عدم حرکت این ماهیچهها، ایلئوس (Ileus) و متعاقب آن، تهوع، استفراغ و انسداد کاذب کلونیک (Pseudo-Obstruction) را ببینیم.

از سایت Radiologykey.com
۳.۳. ماهیچه قلبی
هایپوکالمی در قلب منجر به انواع اختلالات ریتم مثل ضربان زودرس دهلیزی یا بطنی، برادیکاردی سینوسی، تاکیکاردی جانکشنال، بلوک گره دهلیزی بطنی، تاکیکاردی بطنی و فیبریلیشن بطنی میشود. مکانیسم ایجاد این اثرات چیست؟
معادلهی Nernst تعیین میکند که پتانسیل استراحت غشا به چه چیزی وابسته است؟ زمانی که پتانسیل استراحت به حد آستانه برسد، پتانسیل عمل شروع میشود. پتانسیل استراحت غشا به نسبت پتاسیم داخل سلول به پتاسیم خارج سلول بستگی دارد. پس یک کسر در نظر بگیریم که صورت آن پتاسیم داخل سلول و مخرج آن پتاسیم خارج سلول است.

زمانی که پتاسیم خارج سلول کاهش یابد، این نسبت افزایش مییابد. افزایش این نسبت منجر به هایپرپلاریزه شدن غشا شده و سلول سختتر به پتانسیل آستانه برای شروع دپلاریزیشن میرسد. به همین علت شاهد ضعف در ماهیچهی اسکلتی خواهیم بود.
اما این موضوع در قلب متفاوت است. بعضی از سلولهای قلبی، مثل سلولهای فیبر پورکنژ یک کانال به اسم K2P1 دارند. این کانالها به شکل طبیعی، فقط پتاسیم را وارد سلول میکنند. اما زمانی که هایپوکالمی داریم، اتفاق دیگری میافتد؛ در هایپوکالمی کانالهای K2P1 سلولهای پورکنژ، علاوه بر انتقال پتاسیم، سدیم را نیز وارد سلول میکنند. با مثبت شدن داخل سلول، پتانسیل غشا به آستانه رسیده و سلول دپلاریزه میشود. به همین دلیل هایپوکالمی منجر به آریتمی و افزایش تحریکپذیری در قلب میشود.
البته این تنها اثر قلبی هایپوکالمی نیست. هایپوکالمی به واسطهی تنظیم کاهشی (Down-regulation) پمپ سدیم-پتاسیم، موجب کاهش فعالیت آن میشود. به دنبال این کاهش فعالیت، سدیم درون سلول تجمع پیدا میکند و عملکرد تعویضکنندهی سدیم-کلسیم نیز (Na/Ca Exchanger) که از شیب غلظت سدیم برای فعالیت خود استفاده میکند، مختل میشود. در نتیجه کلسیم داخل سلول افزایش مییابد و به دنبال آن فرد مستعد یک سری از آریتمیها از جمله Early afterdepolarizations (EADs) مثل torsades de pointes یا Polymorphic Ventricular Tachycardia میشود.
با اینکه متناقض به نظر میرسد، هایپوکالمی منجر به کاهش سرعت خروج پتاسیم از سلولهای قلبی میشود؛ چون که فعالیت کانالهای پتاسیمی (IKr) توسط هایپوکالمی مهار میشود. اگر پتاسیم خارج سلول کم باشد، این کانالها از روی غشا جمع شده و تخریب میشوند. در نتیجه پتاسیم به آهستگی از سلول خارج میشود و متعاقباً ما QT را به شکل طولانی در نوار قلب خواهیم دید. برخی از صاحبنظران معتقدند که هایپوکالمی با همین مکانیسم تأخیر در رپلاریزاسیون در فیبرهای پورکنژ، منجر به ایجاد موج U در نوار قلب میشود. در هر صورت، در مورد علت ایجاد این موج، توافق وجود ندارد.
پس به طور کلی موارد زیر در نوار قلب فردی که دچار هایپوکالمی است ممکن است دیده شود:
- کاهش ارتفاع ST Segment
- کاهش T wave amplitude
- افزایش U wave amplitude (معمولا در لیدهای V4 تا V6)
- طولانی شدن QT
نکته: در مورد این تغییرات، تفاوت زیادی بین بیماران وجود دارد. ممکن است بیماری با پتاسیم پایینتر این علائم را از خود نشان ندهد اما در بیماری با پتاسیم بالاتر همین علائم بروز کند. این موضوع به فاکتورهای همزمان مثل ایسکمی کرونر یا مصرف برخی داروها از جمله بتابلاکرها بستگی دارد. همچنین هایپوکلمی معمولاً با هایپومنیزیمی همراهی دارد؛ پس سطح منیزیم فرد نیز در بروز علائم هایپوکالمی نقش دارد.
در تصویر زیر تغییرات نوار قلب در هایپوکالمی را در مقایسه با هایپرکالمی میبینید.
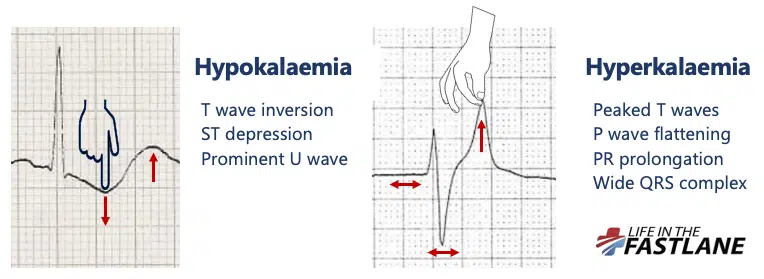
مرور چند نوار قلب
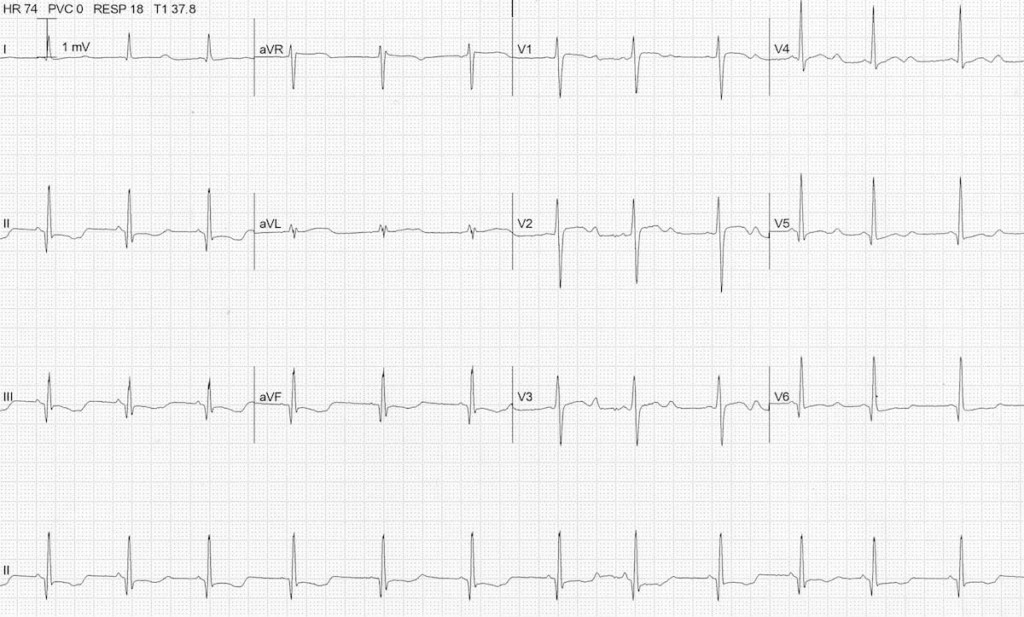
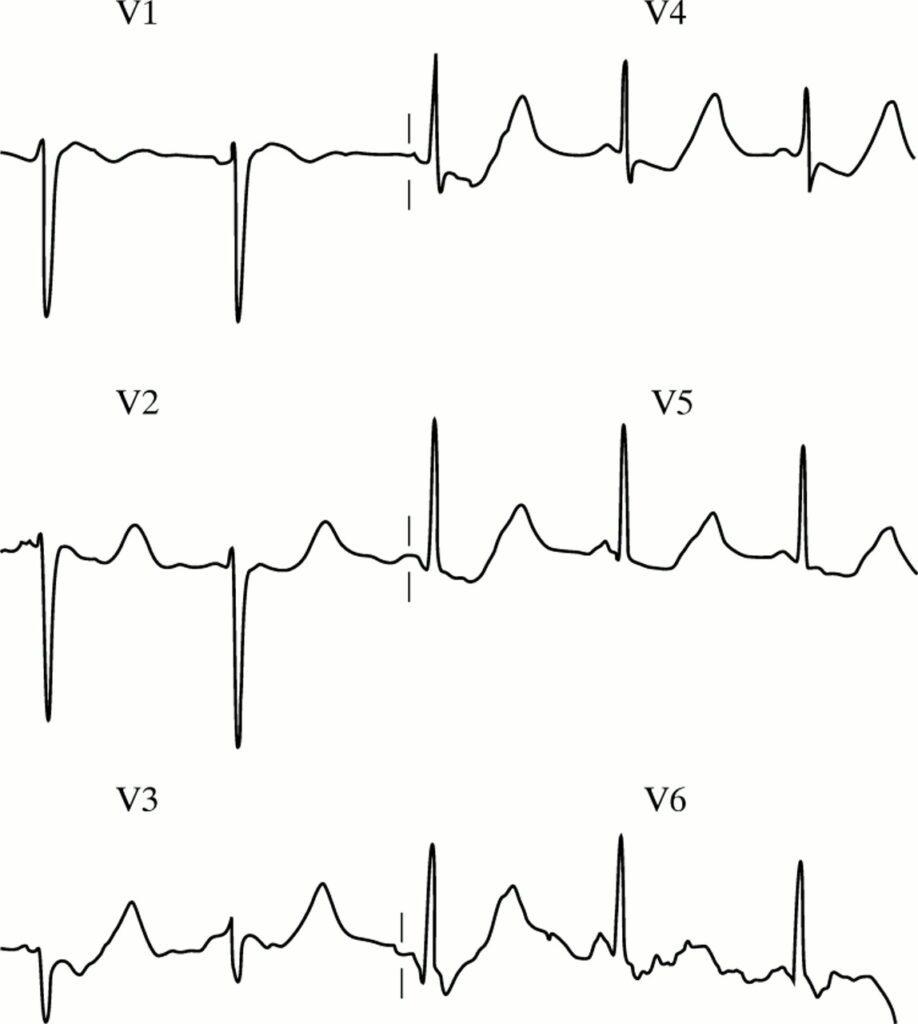
در بررسیها پتاسیم ۱/۸ میلیمول در لیتر داشته است. در نوار قلب شاهد تغییرات معمول نوار قلب به نغع هایپوکالمی هستیم (منبع).
تمرین
کدام دارو را میشناسید که از طریق مکانیسمی مشابه هایپوکالمی، باعث افزایش کلسیم درون سلولهای قلبی میشود.
اختلال الکترولیتی دیگری را که منجر به دیابت بیمزه میشود، نام ببرید.
برای امتیاز دهی به این مطلب، لطفا وارد شوید: برای ورود کلیک کنید





۱- هایپرکلسمی
۲-دیگوکسین