بسیار کملطفی خواهد بود که از تونیسیته و اهمیت سدیم در تونیسیته مایع خارج سلولی بگوییم و معادله ادلمن (Edelman equation) را توضیح ندهیم. معادلهای که بیش از نیم قرن از معرفیاش میگذرد. معادلهای که اساس درک اختلالات سدیم شد. سدیمی که اختلالات آن، شایعترین اختلال الکترولیتی است.
هجدهمین تلاشِ ایزیدور ساموئل ادلمن
ایزیدور ساموئل ادلمن (Isidore Edelman)، در سال ۱۹۲۰، از مادر و پدری مهاجر به نیویورک، به دنیا آمد. دوستانش او را ایزی صدا میکردند.
مادرش دوست داشت که او وکیل بشود. دانشکده پزشکی را زیادی خشن میدانست (+). خودش میگفت که او از معدود یهودیزادههایی بود که والدینش نمیخواستند پسرشان پزشک شود.
ادلمن در ابتدا شیمی خواند و پس از گرفتن لیسانس در شیمی، برای ادامهی تحصیل در پزشکی اقدام کرد.
هفده دانشکده پزشکی درخواست او را رد کردند. هجدهمین تلاش او پذیرفته شد (+).
در طول آن سالها، ادلمن به دو رشته روانپزشکی و طب داخلی علاقه پیدا کرد. اما مشابه ورود او به پزشکی، در هنگام درخواست برای دوران تخصص نیز – با وجود نمرههای درخشان و سابقهی تحصیلی خوب – در جایی پذیرفته نشد.
نمیدانیم اگر ادلمن در آن زمان در رزیدنسی پذیرفته میشد، مسیرش چگونه بود. اما یک چیز از سابقهی او مشخص است. معادلهای که در مورد سدیم به آن رسید، حاصل رد شدنش در برنامههای دستیاری او بود.
او به واسطهی آشنایی با یک کتابدار به یک پزشک دیگر معرفی شد و آن پزشک، او را به پزشکی دیگر معرفی کرد و در نهایت به عنوان دستیار پژوهشی – بدون حقوق – شروع به کار کرد.
در آنجا، یک مسئلهی دیگر به وجود آمد. شروع یک پروژهی مرتبط با تحقیقات اتمی و در نهایت آشنایی با ایزوتوپها و استفاده از آنها برای رسیدن به معادلهای بود که اساس درک سدیم و آب شد. معادلهای که ترکیب بدن را توضیح میدهد.
میشود گفت که معروفترین معادلهی سدیم، مدیون رد شدنهای پیاپی ایزی ادلمن است.

عوامل مؤثر بر غلظت سدیم سرم
ادلمن با مطالعهای که در سال ۱۹۵۸ انجام داد، نشان داد که غلظت سدیم در آب سرم1، به کل آب بدن – و نه فقط میزان آب خارج سلولی – و همچنین مجموع سدیم و پتاسیم بدن – و نه فقط سدیم بدن – بستگی دارد (+).
شاید این حرف او در نگاه اول عجیب باشد. سدیم سرم چرا باید به کل آب بدن مربوط باشد؟ پتاسیم چطور؟ چه ربطی به پتاسیم دارد؟
برای درک این موضوع، در ابتدا شکل سادهشدهی معادله ادلمن را بررسی کنیم. این شکل را برتن رز معرفی کرد (+). معادله کامل ادلمن پیچیده است و ممکن است شما را از این نوشته فراری بدهد. اما پس از توضیحات اولیه و گفتن معادله اصلی متوجه میشوید که نگاه ادلمن، چقدر دقیق است.
فرمول رز (شکل سادهشدهای از ادلمن)
رز در مقالهی سال ۱۹۸۶ خود، شکل سادهشدهای از معادله ادلمن را معرفی کرد. این معادله میگوید که غلظت سدیم سرم به غلظت کل سدیم بدن و غلظت کل پتاسیم بدن و مقدار آب کل بدن بستگی دارد..
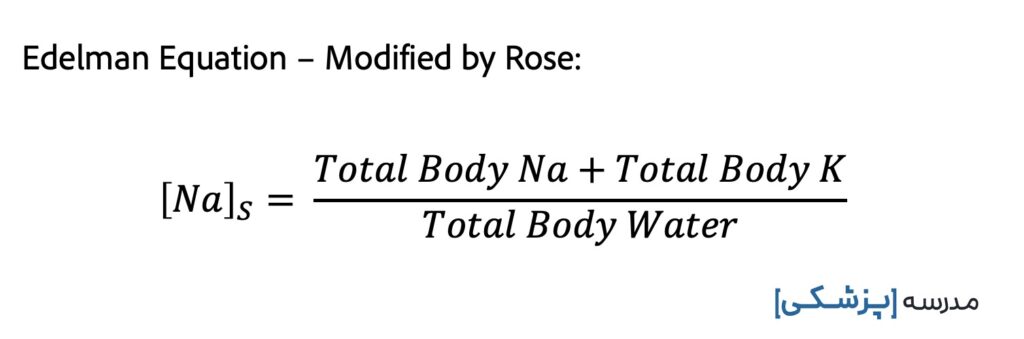
چرا سدیم و پتاسیم؟ چرا دیگر یونها نه؟
کل بدن را همانند یک محفظهی بزرگ در نظر بگیرید که توسط غشایی نفوذپذیر به آب و نفوذناپذیر به یونها، به دو بخش تقسیم شده است. میدانیم که آب آنقدر جابهجا شده که اسمولالیته در دو طرف برابر شود (اصل اسموتیک پیتر یا Peter’s osmotic principle).
این دو بخش در بدن، فضای داخل سلولی و فضای خارج سلولی هستند. بیشترین یونها در این فضا چه هستند؟ سدیم و آنیونهای همراهش در فضای خارج سلولی و پتاسیم و آنیونهای همراهش در فضای داخل سلولی.
با کمی چشمپوشی، میتوانم بگویم که جابهجایی آب بین سلول و بیرون آن، به پتاسیم و سدیم – و آنیونهای همراه آن – وابسته است. زیرا این دو یون هستند که بیشترین ذرات حلشده در آب را در بدن تشکیل میدهند.
حالا برای پاسخ دادن به سؤالهای فوق، فرض کنید که غلظت پتاسیم را در داخل سلول بیشتر کردهایم. آب از سمت سدیم (خارج سلول) به سمت پتاسیم (داخل سلول) رفته تا اسمولالیته دو طرف برابر بشود. پس در نتیجه در سمت سدیم، آب کمتری خواهد بود و غلظت سدیم بیشتر خواهد شد.
بالعکس، اگر پتاسیم کم بشود، آب به سمت سدیم خواهد آمد و غلظت سدیم کمتر خواهد شد.
میبینیم که در نهایت کل آب بدن مؤثر است – زیرا که آب به راحتی جابهجا شده و به یک بخش محدود نیست. از طرفی اثر پتاسیم را هم متوجه شدیم.
ادلمن یک فرضیه داشت: غلظت مواد (غلظت، نه تعداد ذرات) در دو طرف غشای سلولی برابر است. الان متوجه میشویم که فرضیهی او درست بود و توانست این فرضیه را با آزمایش خود به کمک دوتریوم، اثبات کند.
به همین خاطر است که گفته میشود اگر در هنگام هایپوکالمی2 و هایپوناترمی همزمان، هایپوکالمی را درمان کنیم، هایپوناترمی نیز کمتر خواهد شد.
سدیم و پتاسیم قابل تبادل
وقتی معادله اصلی ادلمن را بررسی کنیم، عبارت قابل تبادل (exchangeable) را نیز میبینیم. قبل از بررسی معادله اصلی، بهتر است منظور از قابل تبادل را مشخص کنیم.
سدیم بدن انسان به دو شکل است: (۱) سدیم قابل تبادل (exchangeable) و (۲) سدیم غیر قابل تبادل.
قبل از گفتن این مفهوم، سعی میکنیم آن را با یک آنالوژی بهتر توضیح بدهیم. بهترین آنالوژی ممکن نیست؛ اما به خاطر ملموس بودن، کمک میکند.
در مورد کلسیم میدانیم که قسمت عمدهی کلسیم بدن در استخوان و دندان قرار دارد. از مقداری که در خون وجود دارد، تقریباً نیمی از آن به آلبومین و یونهای منفی متصل است. کلسیم آزاد خون و کلسیم متصل به راحتی با هم تبادل دارند (exchangeable).
اما بدون حضور هورمونهایی مثل پاراتورمون، کلسیم آزاد خون و کلسیم استخوان نمیتوانند به راحتی تبادل داشته باشند.
کلسیم استخوان را میتوانیم شکل ذخیرهای در نظر بگیریم که در حالت عادی قابل تبادل نیست. و میدانیم که بین این سه حالت کلسیم، فقط کلسیم آزاد است که از لحاظ فیزیولوژیک بر روی عملکرد سلول اثر دارد.
شبیه به این حالت برای سدیم نیز وجود دارد.
کل سدیم بدن به دو حالت قابل تبادل و غیر قابل تبادل است. شکی نیست که مثلاً در ساختار اصلی برخی قسمتها وجود دارد، نقشی در فعالیت اسمزی ندارد. اما قسمت قابل تبادل، تقریباً شبیه به کلسیم متصل به آلبومین و یونها و کلسیم آزاد است.
به بیان دیگر مقداری از سدیمهای متصل به مواد دیگر (مثلاً پروتئینها) میتوانند در شرایطی با سدیم آزاد بافتها تبادل داشته باشند و مقداری از این سدیم قابل تبادل نیست.
مثلاً سدیم متصل به برخی از پروتئینهای پلیآنیونیک موجود در پوست، ماهیچه، غضروف، استخوان و لایهی سطحی اندوتلیوم، از جنس سدیم قابل تبادل بوده که در حالت عادی به علت وصل بودن به این پروتئینها، از لحاظ اسمزی یک ذرهی جدا و فعال محسوب نمیشوند (+).
فعالیت اسمزی سدیم، به خاطر سدیم آزاد است.
همچنین مطالعهی Cameron و همکاران با عنوان Evidence That a Major Portion of Cellular Potassium Is Bound نشان داده که قسمت قابل توجهی از پتاسیم داخل سلول نیز متصل به آنیونهای منفی است و در نتیجه اثر اسمزی آن کاهش پیدا میکند.
به خاطر اهمیت قابل تبادل بودن، اندکس E را که مخفف Exchangeable است، در معادلات مربوط به سدیم زیاد میبینیم. تعدادی نیز در معادله ساده شده ادلمن، به جای total body Na/K از عبارت NaE به معنای سدیم قابل تبادل و KE به معنای پتاسیم قابل تبادل استفاده میکنند.

معادله ادلمن
این قسمت تنها برای کسانی است که به مبحث سدیم علاقه بیشتری دارند. بدون دانستن معادله کامل ادلمن هم تقریباً تمام نیاز شما برطرف خواهد شد. شما میتوانید بدون خواندن این قسمت، مستقیماً به درس بعدی بروید.
معادله اصلی ادلمن به شکل زیر است:
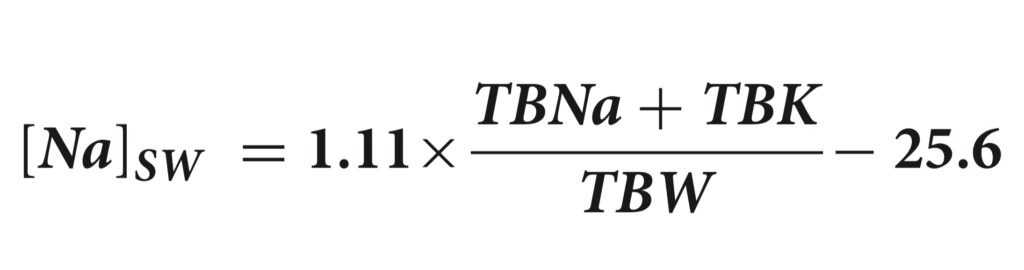
این معادله را میتوان یک معادلهی خطی y = mx+b در نظر گرفت. در شکل سادهشده، شیب (m) برابر با یک در نظر گرفته شده و عرض از مبدأ (Intercept یا همان b) نیز صفر در نظر گرفته شده است. اما در واقعیت این طور نیست.
مطالعهی Nguyen و Kurtz نشان داد که شیب ۱/۱۱ که به روش تجربی به دست آمده بود، به علت اثر مشترک Osmotic Coefficient و Gibbs-Donnan است. همچنین مطالعهی این دو نفر علت وجود عرض از مبدأ به میزان (۲۵/۶) را نیز مشخص کرد.
به نظر میآید که این عدد از عوامل زیر تأثیر گرفته است: (۱) دیگر اسمولهای مؤثر غیر از سدیم و پتاسیم، (۲) میزانی از سدیم و پتاسیم قابل تبادل (exchangeable) که از لحاظ اسمزی فعال نیست و (۳) پتاسیم پلاسما.
توضیح کامل این موارد، درسهای جداگانه نیاز دارد. مباحث سدیم و پتاسیم پر از پیچیدگیهای جالب است. اما یک مورد را میتوانیم به شکل کوتاه در اینجا شرح دهیم. شاید برای شما عجیب باشد که چرا پتاسیم پلاسما اثر کاهشی به روی غلظت سدیم دارد (عرض از مبدأ منفی است)؟
دلیلش را Nguyen و Kurtz اینگونه شرح دادهاند که پتاسیم موجود در مایع بین سلولی و داخل سلول، همانند سدیم، از لحاظ اسمزی فعال بوده و آب به آن سمت میرود. در نتیجه میزان آب بیشتری به سمت مایع میانبافتی و داخل سلول رفته و غلظت سدیم پلاسما بالا میرود.
عکس این اثر برای پتاسیم پلاسما وجود دارد. اما از آنجایی که هنگام کاهش پتاسیم پلاسما، کل ذخایر بدن معمولاً به میزان قابل توجهی کم شده است، اثر کاهش پتاسیم را معادل کاهش کل پتاسیم بدن در نظر گرفته که اثر کاهشی بر سدیم پلاسما دارد.
- ادلمن به شکل بسیار دقیقی از عبارت آب سرم استفاده کرد و نه کل سرم. فکر میکنیم علتش را میتوانید با توجه به تفاوت اسمولالیته و اسمولاریته حدس بزنید. وقتی از آب سرم میگوییم، اسمولالیته میشود و وقتی از کل سرم میگوییم، اسمولاریته. سرم یک فاز آبی و یک فاز غیر آبی دارد. فقط فاز آبی، حاوی سدیم است. در حالت طبیعی، ۹۳ درصد حجم سرم، فاز آبی است و به همین خاطر، سدیم کل سرم از سدیم آب سرم کمتر است و ۹۳ درصدِ سدیم آب سرم میشود. مثلاً اگر سدیم آب سرم ۱۵۰ میلیمول در لیتر باشد، سدیم کل سرم برابر ۱۵۰ * ۰/۹۳ شده که تقریباً ۱۴۰ میلیمول در لیتر خواهد شد. ↩︎
- خوب است بدانیم که هر یک میلیمول در لیتر کاهش پتاسیم خارج سلولی – اگر که به خاطر آمدن پتاسیم به داخل سلول نباشد – معادل حدود ۳۰۰ تا ۴۰۰ میلیمول کاهش پتاسیم کل بدن است. ↩︎
پیام درس
عامل اصلی مؤثر در تونیسته مایع خارج سلولی، غلظت سدیم خارج سلولی است و غلظت سدیم خارج سلولی، تابعی از معادله ادلمن.
مطالعه ادلمن به ما نشان داد که سدیم سرم از ارتباط بین کل سدیم بدن، کل پتاسیم بدن و کل آب بدن به دست میآید و ارتباط آن سه را در معادلهای ترسیم کرد.
در معادله ادلمن، سدیم و پتاسیم قابل تبادل اهمیت دارد. سدیم و پتاسیم بدن انسان به دو شکل است: قابل تبادل و غیرقابل تبادل. آنهایی که قابل تبادل هستند، به دو صورت آزاد (حل شده در مایع داخل یا خارج سلولی) و متصل (به پروتئینها و آنیونهای دیگر) هستند. تنها قسمت آزاد این یونها از لحاظ اسمزی یک ذرهی جدا و فعال محسوب میشوند.
نتیجهگیریهایی که از معادله ادلمن میشود استخراج کرد، اساس درک اختلالات سدیم و درمان آن است که در درس بعدی به آنها میپردازیم.
تمرین درس
با توجه به معادله ادلمن شرح دهید که چرا در SIADH هایپوناترمی داریم. مفهوم SIADH در درسهای فارماکوپاتوفیزیولوژی کلیه گفته شده است.
تا وقتی که در این درس کامنت نگذارید، نمیتوانید کامنت بقیهی دوستان را ببینید.
ترتیبی که مدرسه پزشکی برای مطالعهی درسهای این مجموعه پیشنهاد میدهد، به صورت زیر است:
برای امتیاز دهی به این مطلب، لطفا وارد شوید: برای ورود کلیک کنید




3 کامنت در نوشته «معادله ادلمن | عوامل مؤثر بر غلظت سدیم سرم»