در درس رویکرد تشخیصی در آمبولی ریه به طور مفصل به سختیها و موانع موجود در راه تشخیص آمبولی ریه پرداختیم؛ از خطاهای شناختی پزشکان گرفته تا محدودیتهای موجود در روشهای تشخیصی آزمایشگاهی.
بحث مدیریت و درمان آمبولی ریه ابعاد مختلفی دارد که باید به آن توجه کنیم. جزئیات فراوانی هم هست که همگی در یک نوشته نمیگنجند. در این درس تنها به تعریف چارچوبی کلی برای درمان میپردازیم.
در صورتی که در مرکزی با شیوع بالای آمبولی ریه درس میخوانید یا کار میکنید حتماً به اطلاعات و جزئیات دیگری هم برای درمان نیاز خواهید داشت که به تدریج در مدرسه پزشکی دربارهشان مینویسیم.
ارزیابی و احیا بیماران
هدف اول ما در درمان فردی که به آمبولی ریه شک داریم، در کنار اقدامات تشخیصی که همزمان انجام میدهیم، پایدار کردن وضعیت بیمار از نظر همودینامیک و تنفسی است.
اگر شک زیادی به آمبولی ریه داریم بهتر است قبل از قطعی شدن تشخیص، درمان را شروع کنیم. به تأخیر افتادن درمان تا انجام سیتی آنژیوگرافی ریه میتواند نتایج مصیبت باری به همراه داشته باشد. این موضوع خصوصاً در وضعیت شلوغی اورژانسهای کشور ما، اهمیتش دو چندان میشود.
البته ملاحظاتی هم وجود دارد که باید در نظر داشته باشیم که در ادامه توضیح میدهیم.
ارزیابی وضعیت همودینامیک
ابتدا باید بررسی کنیم که بیمار از نظر همودینامیک در چه وضعیتی قرار دارد.
تعریف ناپایداری همودینامیک (hemodynamic instability) به صورت زیر است:
۱. ایست قلبی، یا
۲. هایپوتنشن به صورت فشار خون سیستولیک کمتر از ۹۰ میلیمتر جیوه یا اینکه برای بالا نگه داشتن فشار خون سیستولیک بالاتر از ۹۰ نیازمند داروهای وازوپرسور باشیم، یا
۳. فشار خون کمتر از ۹۰ میلیمتر جیوه به صورت مداوم یا افت بیشتر یا مساوی ۴۰ میلیمتر جیوه از فشار خون پایهی بیمار که بیشتر از ۱۵ دقیقه طول بکشد، به شرط اینکه علت افت فشار خون، آریتمی، هایپوولمی یا سپسیس نباشد.
هر بیماری که شرایط بالا را نداشت، از نظر همودینامیک پایدار به حساب میآید (hemodynamically stable).
این موضوع را به یاد داشته باشیم که ممکن است بعد از احیا اولیه و شروع درمان حمایتی، بیماران بر اساس وضعیت بالینیشان از گروهی به گروه دیگر منتقل شوند و مسیر درمانشان عوض شود.
مثلاً بیماری که ابتدا فشار خون پایینی داشته و سپس با احیا با مایعات فشارش به حد طبیعی میرسد دیگر در گروه با ریسک مرگ و میر بالا قرار ندارد. یا بیماری که در ابتدا به عنوان ریسک پایین درمان میشد، اگر ناگهان دچار افت فشار خون شود که نیاز به وازوپرسور برای بالا نگه داشتن فشار خونش داشته باشیم، به گروه با ریسک بالای مرگ و میر ارتقا مییابد.
اقدامات درمانی اولیه
بعد از ارزیابی وضعیت همودینامیک در ابتدا مجموعهای از اقدامات برای همهی بیماران انجام میشود:
حمایت تنفسی
حمایت تنفسی با هدف رساندن درصد اشباع اکسیژن بالای ۹۰٪ ضروری است. عمدتاً با یک ماسک ساده یا اکسیژن با نازال کانولا کفایت میکند؛ اما اگر بیمار هیپوکسمی شدید دارد یا دچار نارسایی تنفسی شده یا کاهش هشیاری قابل توجه دارد، اینتوبه کردن ضروری است.
اینتوبه کردن این بیماران که خود در معرض اختلال عملکرد بطن راست هستند چالش بزرگی است؛ چرا که ریسک افت فشار خون به دنبال اینتوبه شدن وجود دارد.
چرا؟
تنفس عادی از جنس فشار منفی است. در توراکس فشار منفی (نسبت به فشار اتمسفر) ایجاد شده و فشار داخل آلوئول منفی میشود. این اختلاف فشار منجر به جاری شدن هوا از دهان (فشار هوا) به آلوئول (فشار کمتر از هوا) خواهد شد.
اما در زمان اینتوبه بودن، تنفس با فشار مثبت است. یعنی اختلاف فشار لازم برای جاری شدن هوا را، با مثبتتر کردن فشار در قسمت فوقانی دستگاه تنفس (دهان یا نای) انجام میدهیم. این فشار مثبت به ساختارهای داخل قفسه سینه از جمله وریدهای بزرگ و قلب هم وارد شده و بازگشت وریدی را کاهش می دهد که میتواند منجر به افت فشار خون شود.
حمایت همودینامیکی
حمایت همودینامیکی در بیماران ضروری بوده و نیازمند دقت فراوانی است. یادمان باشد که عدد فشار خون نباید خیالمان را در این باره راحت کند. فشار خون بیمار را با فشار خون پایه خودش مقایسه کنیم و برای اقدامات لازم معیار قرار بدهیم.
معیارهای بالینی دیگری که باید مد نظر داشته باشیم، هایپوپرفیوژن ارگانها است – مثلاً کاهش حجم ادرار و تغییر وضعیت هوشیاری.
درمان هایپوتنشن در ابتدا دادن مایعات وریدی است. بهتر است مایعات را با حجم کم و احتیاط فراوان تجویز کنیم و مرتباً وضعیت فشار خون بیمار را در پاسخ به مایعات تجویزی ارزیابی کنیم.
میتوانیم مایعات وریدی را در حجمهای کم در حد ۲۵۰ تا ۵۰۰ میلی لیتر و معمولاً نرمال سالین تجویز کنیم.
دادن حجمهای زیاد مایع با بیشتر کردن پرهلود میتواند فشار به روی بطن راست را زیادتر کرده و باعث ایسکمی و اختلال عملکرد بطن راست شود.
علاوه بر این، به این موضوع توجه کنیم که سپتوم بین دو بطن، یک دیوارهی متحرک است. در آمبولی ریه، به خاطر مسدود شدن مسیر خروجی بطن راست به خاطر لخته، فشار بطن راست بالا میآورد. این افزایش فشارِ حاد، سپتوم را به سمت بطن چپ هل خواهد داد. در نتیجه فضای بطن چپ محدود شده و ممکن است منجر به کاهش خروجی بطن چپ (LV EF) شود.
اگر با دادن مایع به شکل محدود وضعیت فشار خون بیمار و پرفیوژن ارگانها بهتر نشد، دادن وازوپرسور وریدی را در نظر داشته باشیم. اینکه کدام وازوپرسور ارجح است به فاکتورهای زیادی بستگی دارد که توضیح آن در این نوشته نمیگنجد.
اما به صورت کلی در آمبولی حاد ریه داروی نور اپینفرین را ترجیح میدهیم. نسبت به بقیه وازوپرسورها، نور اپینفرین بیماران را کمتر تاکیکارد میکند.
ترجیح میدهیم در این شرایط از تاکیکاردی دوری کنیم؛ زیرا میتواند هایپوتنشن آنها را بدتر کند.
چرا؟
بطن در زمان دیاستول پر میشود و تاکی کاردی با کاهش زمان دیاستول، اجازهی پر شدن به بطن نمیدهد. در نتیجه منجر به کاهش خروجی بطن چپ (LV EF) خواهد شد و فشار خون کاهش مییابد.
شروع آنتیکواگولان قبل از تأیید تشخیص
این که برای چه کسی آنتیکواگولان شروع میکنیم به عوامل مختلفی از جمله شک بالینی به آمبولی ریه (بر اساس معیار تعیین ریسک ولز)، ریسک خونریزی و مدت زمانی که طول میکشد اقدامات تشخیص قطعی انجام شود، بستگی دارد.
استراتژی درمانی که توسط آپتودیت پیشنهاد شده به صورت زیر است. شکل کاربردی آن را نیز پس از این معیارهای آپتودیت نوشتهایم:
- اگر خطر خونریزی پایین باشد، بیماران بر اساس امتیاز کسب شده در معیار تشخیصی ولز به صورت زیر برایشان تصمیمگیری میشود:
- اگر امتیاز بیشتر از ۶ باشد یا شک بالینی بالایی برای آمبولی ریه وجود داشته باشد، درمان با آنتیکواگولان قبل از تأیید شدن تشخیص شروع میشود.
- اگر امتیاز بین ۲ تا ۶ باشد، تنها در صورتی آنتیکواگولان شروع میکنیم که تکمیل اقدامات تشخیصی بیشتر از ۴ ساعت طول بکشد.
- اگر امتیاز ولز صفر یا یک باشد، تنها در صورتی آنتیکواگولان شروع میکنیم که تکمیل اقدامات تشخیصی به بیشتر از ۲۴ ساعت زمان نیاز داشته باشد.
- اگر بیمار برای تجویز آنتیکواگولان هرگونه کنترا اندیکاسیونی داشته باشد (مثلاً سکته هموراژیک اخیر) یا خطر بالایی برای خونریزی داشته باشد، روشهای جایگزینی را در نظر میگیریم (مثل گذاشتن فیلتر ورید اجوف تحتانی یا روشهای جراحی آمبولکتومی)
- اگر بیمار در این دو گروه بالا جای نگیرد، باید بر اساس وضعیت بالینی بیمار و بیماری زمینهای و سبک سنگین کردن شرایط، در مورد شروع آنتیکواگولان تصمیمگیری میکنیم.
اگر شک بالا باشد، منتظر تست نمیمانیم و شروع میکنیم. اگر شک متوسط بوده ولی بررسی های تأییدکننده در دسترس نباشد، میتوانیم درمان را شروع کنیم. هر چند در هر دو حالت باید ریسک خونریزی را در نظر بگیریم.
انتخاب داروی آنتیکواگولان
این که کدام داروی آنتیکواگولان را انتخاب میکنیم نیاز به در نظر گرفتن شرایط متعددی از جمله ویژگیهای دارو، در دسترس بودن آن، کنترا اندیکاسیونهای هر کدام، بیماریهای زمینهای و کارکرد کلیه و کبد بستگی دارد که توضیح کامل آن را به درسی دیگر موکول میکنیم.
فعلاً موارد زیر را به خاطر داشته باشید:
به صورت کلی، اگر بیمار شرایطی داشته باشد که بخواهیم از داروهای آنتیکواگولان خوراکی استفاده کنیم، داروهای آنتیکواگوالان خوراکی با اثر مستقیم (direct oral anticoagulants یا DOACs) که شامل دو خانواده مهارکنندههای مستقیم ترومبین و مهارکننده فاکتور ۱۰ فعال است، نسبت به داروهای آنتاگونیست ویتامین K (مثل وارفارین) ارجح هستند. چرا که مؤثرتر و مطمئنتر بوده و استفاده از آنها نیز برای بیماران راحتتر است.
در کشور ما مهارکنندههای فاکتور ۱۰ فعال مثل آپیکسابان و ریواروکسابان در دسترستر و ارزانتر از مهارکنندههای مستقیم ترومبین مثل بیوالیرودین، آرگاتروبان و دابیگاتران هستند.
در بیمارانی که در زمینهی سرطان دچار ترومبوز شدهاند بهتر است از هپارین با وزن مولکولی پایین (Low-molecular-weight-heparin یا LMWH) مثل انوکساپارین استفاده کرد. این بیماران اگر ریسک بالایی برای خونریزی گوارشی یا ادراری – تناسلی نداشته باشند، میتوانیم از مهارکنندههای فاکتور ۱۰ فعال مثل آپیکاسابان و ریواروکسابان استفاده کنیم. انوکساپارین تزریقی است و استفادهی طولانی مدت از آن، برای بیمار دشوار است.
بیمارانی که شرایط آنها ایجاب میکند که از داروهای تزریقی استفاده کنیم، LMWH مثل انوکساپارین نسبت به unfractionated heparin یا UFH ارجح است.
اولاً تزریق انوکساپارین بسیار راحتتر بوده و حداکثر دو بار در روز تزریق میشود و نیاز به انفوزیون دائم مثل هپارین عادی ندارد. دوماً نیاز به آزمایش گرفتن برای بررسی اثر آن نیست. زیرا برخلاف هپارین معمولی که فارماکوکینتیک غیر قابل پیشبینی دارد، اثر آن قابل پیشبینیتر است.
اما چند موقعیت است که بهتر است به سراغ همان هپارین برویم:
- بیمارانی که عملکرد کلیه آنها به شکل جدی مختل است (یعنی GFR کمتر از ۳۰ دارند) بهتر است از unfractionated heparin استفاده کنیم؛ زیرا امکانات بررسی کردن اثر انوکساپارین برای ما در دسترس نیست.
- در بیمارانی که ریسک خونریزی نسبتاً بالایی دارند، بهتر است از هپارین معمولی استفاده کنیم؛ زیرا اثر آن بسیار سریعتر نسبت به انوکساپارین از بین خواهد رفت.
- در افرادی که BMI بیشتر از ۴۰ دارند، اثر انوکساپارین پیشبینیناپذیر است و با توجه به نداشتن امکانات بررسی اثر آن، بهتر است به سراغ هپارین برویم.
- قیمت انوکساپارین نسبت به هپارین – در افرادی که بیمه ندارند – بسیار بیشتر است. هر چند اگر قرار باشد با پمپ انفوزیون تزریق شود، هزینه آن را نیز باید در نظر گرفت.
به صورت کلی در بیماری که اپیستاکسی دارد، به دلیل عادت ماهیانه خونریزی واژینال دارد یا هموپتزی خفیف (که در زمینه آمبولی ریه نیز میتواند رخ دهد)، تجویز آنتیکواگولان ممنوع نیست؛ ولی باید آنها را حین دریافت درمان به دقت تحت نظر بگیریم.
درمان در بیمارانی که تشخیص آمبولی تأیید شده است
در گایدلاینهای مختلف رویکردهای متفاوتی در قبال درمان بیماران با تشخیص قطعی آمبولی ریه وجود دارد. البته که کلیات آنها مشابه است و تفاوت زیادی با یکدیگر ندارند. در مدرسه پزشکی ما بر اساس رویکرد نویسندگان آپتودیت پیش رفتهایم؛ چرا که رویکرد سادهتری است و پیچیدگیهای تقسیمبندی گایدلاین European Society of Cardiology را ندارد.
عمدهی اختلاف در درمان ترومبولیتیک در فرد با وضعیت هموداینامیک پایدار است. سؤال این است که چه افراد دیگری به جز بیماران با هموداینامیک ناپایدار، از ترومبولیز سود خواهند برد؟ از آنجایی که داروی فیبرینولیز در این افراد به اندازه هموداینامیک ناپایدار اورژانسی نیست و همچنین تا ۱۴ روز فرصت است، ما در این درس دغدغهی پرداختن به این افراد را نداریم.
همانطور که بالاتر توضیح دادهایم، درمان بر اساس وضعیت همودینامیک بیمار انتخاب میشود: همودینامیک پایدار و همودینامیک ناپایدار.
بیماران با همودینامیک ناپایدار (Hemodynamically Unstable)
این قسمت یک پیام مهم دارد و همان را باید به یاد داشته باشیم. بیمار با هموداینامیک ناپایدار باید فیبرینولیز بگیرد؛ مگر دارو را نداشته باشیم یا بیمار شرایطش را نداشته باشد.
این دسته را معادل massive emboli یا از نظر خطر مرگ و میر High-risk در نظر میگیریم. بیمارانی که از نظر همودینامیک در شرایط ناپایداری هستند و آنهایی که علیرغم درمان با آنتیکواگولان شرایطشان وخیمتر میشود، کاندید دریافت ترومبولیتیک سیستمیک هستند.
اگر بیماران ممنوعیتی برای دریافت داروهای ترومبولیتیک داشته باشند یا اینکه بعد از دریافت ترومبولیتیک وضعیتشان تغییری نکرده است، باید روشهای جراحی مثل آمبولکتومی را در نظر داشته باشیم.
در درسی جداگانه به نحوهی تجویز ترومبولیتیک میپردازیم.
علاوه بر بیماران با همودینامیک ناپایدار، بعضی شرایط نیز هستند که اندیکاسیونهای بالقوهای برای تزریق ترومبولیتیک محسوب میشوند. این شرایط آنهایی هستند که میتوان به عنوان بمب ساعتی در نظر گرفت چرا که در هر لحظه ممکن است وضعیتشان بدتر شود:
- آنهایی که اختلال شدیدی در عملکرد بطن راست دارند (در دستهبندی ESC در گروه intermediate-high قرار میگیرند)
- هایپوکسمی شدید (خصوصا اگر بیماری قلبی-ریوی همزمان عامل این هایپوکسمی نباشد)
- کسانی که به نظر میرسد وضعیتشان وخیم شود ولی هنوز دچار هایپوتنشن نشدهاند.
- حجم لخته بسیار بزرگ
بیماران با همودینامیک پایدار (Hemodynamically Stable)
بیماران با همودینامیک پایدار شامل طیف گستردهای از بیماران هستند. درست است که این بیماران از نظر ریسک مرگ و میر و خطر بدتر شدن بیماری توسط گایدلاین ESC در دو گروه low-risk و intermediate-risk قرار داده میشود، اما رویکردمان در درمان آنها تقریباً شبیه به هم است:
- اگر ریسک خونریزی در آنها پایین است، درمان با آنتیکواگولان شروع میشود.
- اگر تجویز آنتیکواگولان در بیمار مطلقاً ممنوع باشد، میتوانیم از روشهایی مثل فیلتر ورید اجوف تحتانی (IVC filter) استفاده کنیم. زمانی که تشخیص PE تایید شده باشد و تجویز آنتیکواگولان ممنوع باشد، حتی اگر سایز لخته کوچک باشد و ترومبوزی هم در وریدهای عمقی اندام تحتانی باقی نمانده باشد، باز هم تعبیه فیلتر ضروری است.
- اگر ریسک خونریزی متوسط تا بالا است، پزشک باید درمان را بر اساس فاکتورهای خطر و بیماریهای زمینهای هر فرد، درمان را انتخاب کند که میتواند شامل شروع آنتیکواگولان و یا تعبیه IVC filter باشد.
بعد از شروع آنتیکواگولان باید شرایط بیمار را به دقت زیر نظر بگیریم. در صورت بدتر شدن وضعیت بیمار و ناپایدار شدن همودینامیک، درمان با داروهای ترومبولیتیک و یا روشهای جراحی مثل آمبولکتومی را باید در نظر داشته باشیم.
دستهای از بیماران با همودینامیک پایدار هستند که در مورد شروع درمان با آنتیکواگولان در آنها اختلاف نظر وجود دارد. همچنین دستهای از بیماران را میتوان به صورت سرپایی درمان کرد که در ادامه به آنها میپردازیم.
آمبولی ریه ساب سگمنتال (Subsegmental PTE)
این قسمت را میتوانید نخوانید و از آن بگذرید. آمبولی ساب سگمنتال اولویت یادگیری نیست و قسمت بعدی که درمان سرپایی است، مهمتر است.
اگر لخته در قسمت انتهایی شریان ریوی از انشعاب چهارم به بعد ایجاد شود به آن subsegmental pulmonary embolism یا SSPE میگویند.
سؤال اصلی در آمبولی ساب سگمنتال درمان یا عدم درمان است.
این نوع از آمبولی ریه میتواند محدود به یک شریان باشد (isolated) یا زیرشاخههای متعددی را شامل شود (multiple). میتواند علامتدار یا بدون علامت باشد و همچنین با یا بدون ترومبوز وریدهای عمقی همراه باشد.
برای درمان این دسته از بیماران low-risk در بین گایدلاینهای مختلف، اختلاف نظر وجود دارد. قسمتی از این اختلاف نظر ناشی از نتایج مثبت کاذب قابل توجهی است که در گزارش subsegmental PE در بین رادیولوژیستها وجود دارد (حدود ۵ تا ۲۵٪ سیتی آنژیوگرافیها مثبت کاذباند).
در مطالعات انجام شده دیدهاند که ریسک عود آمبولی در بیماران با SSPE در ۹۰ روز اول بعد از تشخیص حدود ۳٪ است. این میزان در آنهایی که ترومبوزهای سابسگمنتال متعدد دارند یا سنشان بالای ۶۵ سال است، بیشتر است.
پیشنهاد فعلی آپتودیت این است که بیماران مبتلا به SSPE مثل PTE عادی داروی آنتی کواگولان دریافت کنند – مخصوصاً اگر علتی برای PTE یافت نشود.
درمان سرپایی در آمبولی ریه
قبلاً همهی بیماران با تشخیص آمبولی ریه، بستری میشدند. این مربوط به گذشته است. بعد از معرفی داروهای DOAC و راحتی استفاده از آنها، درمان سرپایی بیماران با آمبولی حاد ریه کاملاً امکانپذیر است و رویکردی مطمئن و مؤثر به حساب میآید.
گایدلاینهای معتبر این اجازه را به ما میدهند که بیماران با آمبولی ریوی حاد با ریسک پایین را به صورت سرپایی درمان کنیم.
برای تعیین این گروه از بیماران ابزارهای طبقهبندی متعددی معرفی شدهاند که شامل pulmonary embolism severity index یا PESI و نوع ساده شدهی آن یعنی simplified PESI است. این دو اندکس میزان مورتالینی ۳۰ روزه را با توجه به بیماریهای همراه و ویژگیهای بالینی بیمار تعیین میکنند.
برای آشنایی با این ابزار به توضیحات مربوط به رویکرد درمانی در گایدلاین ESC در کمی پایینتر مراجعه کنید.
معیار دیگری که به طور اختصاصی به این منظور طراحی شده و مورد مطالعه قرار گرفته است، معیار Hestia است که شامل بیماریهای همراه و مسائل سایکوسوشال است.
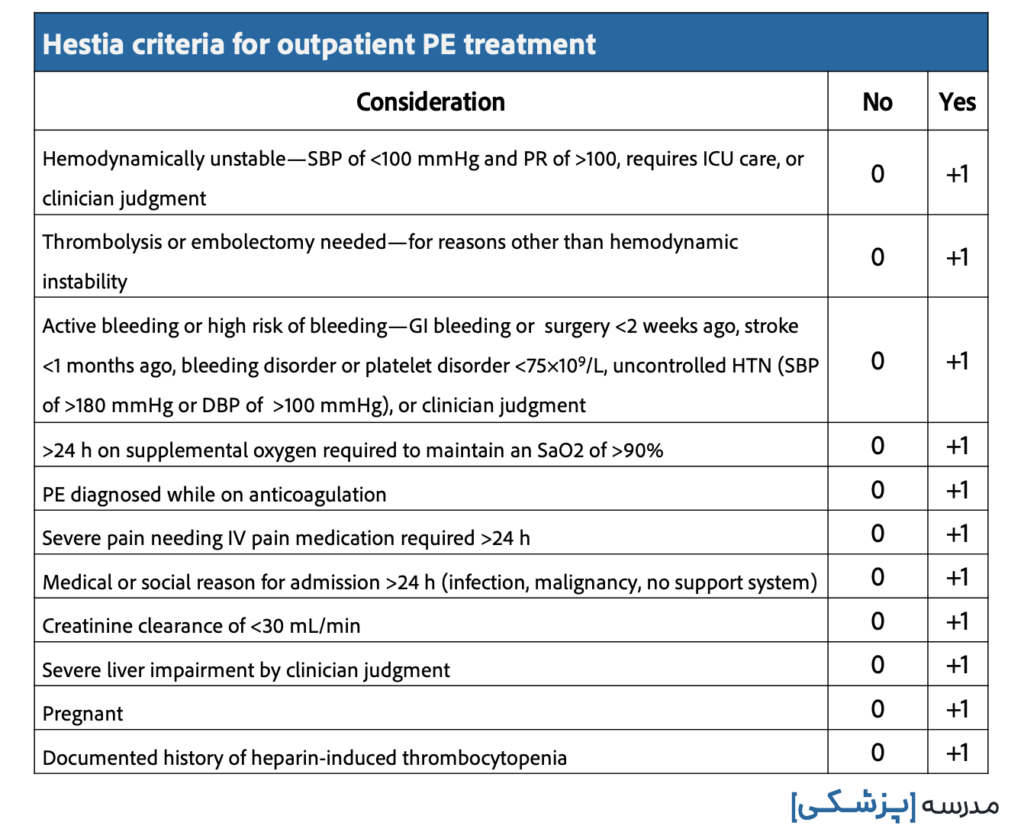
در نهایت یادمان باشد همانطور که آخرین گایدلاین (سال ۲۰۲۱) CHEST برای درمان سرپایی آمبولی تأکید میکند که در هنگام ترخیص باید از مراقبت درمانی کافی در منزل و همچنین دسترسی به امکانات درمانی مطمئن شویم. این موارد همان قسمت روانی – اجتماعی در معیار هستیا بوده که تحت عنوان social reason for admission آورده است.
به همین دلیل پیشنهاد میکنیم برای مشخص کردن آن دسته از بیمارانی که میتوانیم با خیال راحت و با پشتوانهای مبتنی بر شواهد آنها را به صورت سرپایی درمان کنیم، از معیار Hestia استفاده کنیم.
رویکرد گایدلاین انجمن کاردیولوژی اروپا (ESC)
این قسمت از نوشته تنها جهت مطالعهی بیشتر علاقهمندان آورده شده است. تا همین قسمت نیز بیماران PTE را میتوانید به خوبی درمان بکنید. اگر دلتان میخواهد بیشتر بخوانید، قسمت زیر را مطالعه کنید.
رویکرد گایدلاین انجمن کاردیولوژی اروپا (ESC) (برای مطالعه کلیک کنید)
در این گایدلاین درمان آمبولی حاد ریه (acute PE) بر اساس شدت آن (severity) تعیین میشود.
قبلاً برای درمان، آمبولی ریه بر اساس وضعیت همودینامیک و کارکرد بطن راست، به دو دسته کلی massive و submassive تقسیم و درمان میشد (شبیه رویکرد درمانی مطرح شده در ویرایش بیست و یکم کتاب اصول طب داخلی هریسون)، اما ESC تقسیمبندی جدیدتری را پیشنهاد میکنند.
این تقسیمبندی و ترمینولوژی جدیدتر برای درمان آمبولی ریه، بر اساس تعیین خطر مرگ و میر طراحی شده و عمل میکند. حواسمان باشد که این دستهبندی و تعیین ریسک، متفاوت از معیار تعیین ریسک ولز است که در رویکرد تشخیصی از آن استفاده کردیم.
در دستهبندی شدت آمبولی برای تصمیمگیری درباره نحوه درمان بیمار، از مجموعهی پارامترهای بالینی، تصویربرداری و آزمایشگاهی استفاده میکنیم که خلاصهای از آن در جدول زیر آمده است. در ادامه هر کدام را به شکل جداگانه توضیح میدهیم.

معیار PESI و sPESI
برای تعیین ریسک مرگ و میر بیماران با آمبولی ریه و تصمیمگیری درباره نحوه درمان ابزارهای طبقهبندی متعددی وجود دارند که دو تا از معروفترین آنها شامل pulmonary embolism severity index یا PESI و نوع سادهشدهی آن یعنی simplified PESI است.
معیار PESI به دلیل سختی محاسبه و تعدد فاکتورها، خیلی در بالین به کار نمیرود. به جای آن نوع سادهشدهی آن simplified PESI را به کار میبریم که راحتتر بوده و در تعیین ریسک، عملکردی مشابه PESI دارند.

درمان در بیماران با ریسک مرگ و میر بالا (High-Risk PE)
کسانی که در این دسته جای میگیرند آنهایی هستند که از لحاظ همودینامیک شرایطشان ناپایدار است و خطر مرگ و میر بالایی دارند. بالاتر تعریف ناپایداری همودینامیک را توضیح دادیم. برای قرار دادن بیماران در این دسته، به پارامترهای آزمایشگاهی (تروپونین) و اکوکاریوگرافی (وجود شواهد RV strain) نیازی نداریم، اگر چه به احتمال زیاد مثبت باشند.
بیمارانی که بعد از تعیین ریسک مرگ و میر، در دسته high-risk قرار میگیرند یا آنهایی که در دستهی پایینتر قرار دارند ولی علیرغم دریافت آنتیکواگولان شرایطشان وخیمتر میشود، کاندید دریافت ترومبولیز (حل کننده لخته) هستند.
درمان در بیماران با ریسک مرگ و میر متوسط (Intermediate-Risk PE)
این دسته معادل submassive emboli است. آنهایی که از نظر همودینامیک در وضعیت پایداری هستند ولی شواهدی از اختلال عملکرد بطن راست دارند، در این دسته قرار میگیرند.
بر اساس گایدلاین ESC برای انتخاب درمان، بیماران این دسته را به دو زیرگروه ریسک متوسط به بالا (intermediate-high) و ریسک متوسط به پایین (intermediate-low) است.
بیمارانی که هم شواهد اختلال عملکرد بطن راست دارند و هم تروپونین آنها افزایش یافته است، در زیرگروه intermediate-high قرار میگیرند. آنهایی که فقط یکی از این دو مورد را داشته باشند (اختلال عملکرد بطن راست یا تروپونین مثبت) در زیرگروه intermediate-low جای میگیرند.
برای زیر گروه intermediate-low براساس شرایط بالینی از داروهای آنتیکواگولانت خوراکی یا LMWH استفاده میکنیم.
زیر گروه intermediate-high باید در دو تا سه روز اول درمان که بیشترین احتمال برای وخیم شدن وضعیتشان وجود دارد، از هپارین یا LMWH استفاده شود. برای استفاده از ترومبولیتیکها در این زیرگروه اختلاف نظر وجود دارد. با این وجود گایدلاینهای فعلی، استفاده از ترومبولیتیک را فقط در بیمارانی که علیرغم درمان شرایطشان وخیمتر میشود، پیشنهاد میکنند.
از طرف دیگر، استفاده از درمانهای catheter-directed در بیماران قرار گرفته در دستهی intermediate-Risk رو به افزایش است و نتایج خوبی نیز داشته است (بهبود اتساع بطن راست و کاهش فشار شریان ریوی).
درمان در بیماران با ریسک مرگ و میر پایین (Low-Risk PE)
چه بیمارانی در این دسته قرار میگیرند؟
بیمارانی که از نظر همودینامیک شرایط پایداری دارند و در اکوکاردیوگرافی نیز شواهدی از RV strain ندارند. تروپونین آنها نیز منفی خواهد بود. این بیماران در صورت محاسبهی PESI یا simplified PESI ریسک مرگ و میر بالایی نخواهند داشت.
بیماران low-risk PTE را بر اساس شرایط بالینی میتوانیم با LMWH یا داروهای آنتیکواگولان خوراکی درمان کنیم.
پیام درس
اولین اقدام در درمان آمبولی ریه بررسی وضعیت همودینامیک بیمار است.
تعریف ناپایداری همودینامیک (hemodynamic instability) به صورت زیر است:
۱. ایست قلبی، یا
۲. هایپوتنشن به صورت فشار خون سیستولیک کمتر از ۹۰ میلیمتر جیوه یا اینکه برای بالا نگه داشتن فشار خون سیستولیک بالاتر از ۹۰ نیازمند داروهای وازوپروسور باشیم، یا
۳. فشار خون کمتر از ۹۰ میلیمتر جیوه به صورت مداوم یا افت بیشتر یا مساوی ۴۰ میلیمتر جیوه از فشار خون پایهی بیمار که بیشتر از ۱۵ دقیقه طول بکشد، به شرط اینکه علت افت فشار خون آریتمی، هایپوولمی یا سپسیس نباشد.
اگر بیمار این شرایط را نداشت پس در وضعیت پایداری از نظر همودینامیک قرار دارد.
یکسری از اقدامات حمایتی شامل حمایت تنفسی (گذاشتن اکسیژن و در صورت نیاز اینتوباسیون) و حمایت همودینامیکی (تجویز با احتیاط مایع و در صورت نیاز استفاده از وازوپرسورها) برای همه بیماران انجام میشود.
همچنین بر اساس (۱) شک بالینی به آمبولی ریه (بر اساس معیار تعیین ریسک ولز)، (۲) ریسک خونریزی و (۳)مدت زمانی که طول میکشد اقدامات تشخیص قطعی انجام شود، قبل از تأیید تشخیص در مورد شروع آنتیکواگوالان تصمیم میگیریم.
اگر شک بالایی داشته باشیم، منتظر تست نمیمانیم و آنتیکواگولان را شروع میکنیم. اگر شک متوسط بوده ولی آزمایشهایی تأییدکننده در دسترس نباشد، میتوانیم درمان را شروع کنیم. هر چند در هر دو حالت باید ریسک خونریزی را در نظر بگیریم.
اگر بیمار در شرایط پایداری از نظر همودینامیک قرار داشت، عموماً داروهای آنتیکواگولان را برایشان شروع میکنیم. مگر اینکه بیمار برای دریافت دارو ممنوعیتی داشته باشد یا ریسک خونریزی خیلی بالایی داشته باشد که در آن موقع تعبیه فیلتر IVC را در نظر میگیریم.
در مورد شروع آنتیکواگولان در بیماران با آمبولی ریه سابسگمنتال اختلاف نظر وجود دارد.
دستهای از بیماران low-risk هستند که میتوانند درمان با آنتیکواگولان را به صورت سرپایی دریافت کنند. برای مشخص کردن این دسته، از معیار Hestia استفاده میکنیم.
اگر بیمار ناپایدار بود یا علیرغم تجویز آنتیکواگولان شرایطش بهبود نیافت، تجویز داروهای ترومبولیتیک سیستمیک را در نظر میگیریم. اگر هم بیمار کاندید مناسبی برای دریافت ترومبولیتیک نبود یا پاسخ مناسبی به ترومبولیتیک نداد، از روشهای جراحی آمبولکتومی استفاده میکنیم.
تمرین درس
یکی از تجربههای خود در مورد درمان با داروی فیبرینولیز در PTE را برای ما و سایر دوستانتان بنویسید.




